撰稿人:化学系 Brian Wong 和 Dan Fu, University of Washington
结语
Moku:Pro 的锁相放大器 (LIA) 为受激拉曼散射 (SRS) 显微镜实验中的自外差信号检测提供了一种直观、精确且稳健的解决方案。 高质量的 LIA 是 SRS 显微镜实验中具有调制传输检测方案的关键硬件组件。 在此更新的案例研究中,我们提供了有关双 LIA 应用程序的更多详细信息和描述。
什么是受激拉曼散射显微镜?
SRS 是一种相干拉曼散射过程,允许使用光谱和空间信息进行化学成像。1 它使用两个同步脉冲激光器,即泵浦和斯托克斯(图 1)相干地激发分子的振动。 当入射到样品上的两束激光的频率差与目标分子的振动频率相匹配时,就会发生 SRS 过程。 振动激发的结果是泵浦光束将失去光子,而斯托克斯光束将获得光子。 当检测到泵浦光束的损失时,这称为受激拉曼损失 (SRL) 检测。 强度损失 ΔIₚ/Iₚ 通常约为 10-7-10-4,远小于典型的激光强度波动。 为了克服这一挑战,需要一种高频调制和相敏检测方案来从嘈杂的背景中提取 SRS 信号。2 在 SRL 检测方案中,斯托克斯光束以固定频率调制,由此产生的调制传输到泵浦光束由 LIA 检测。
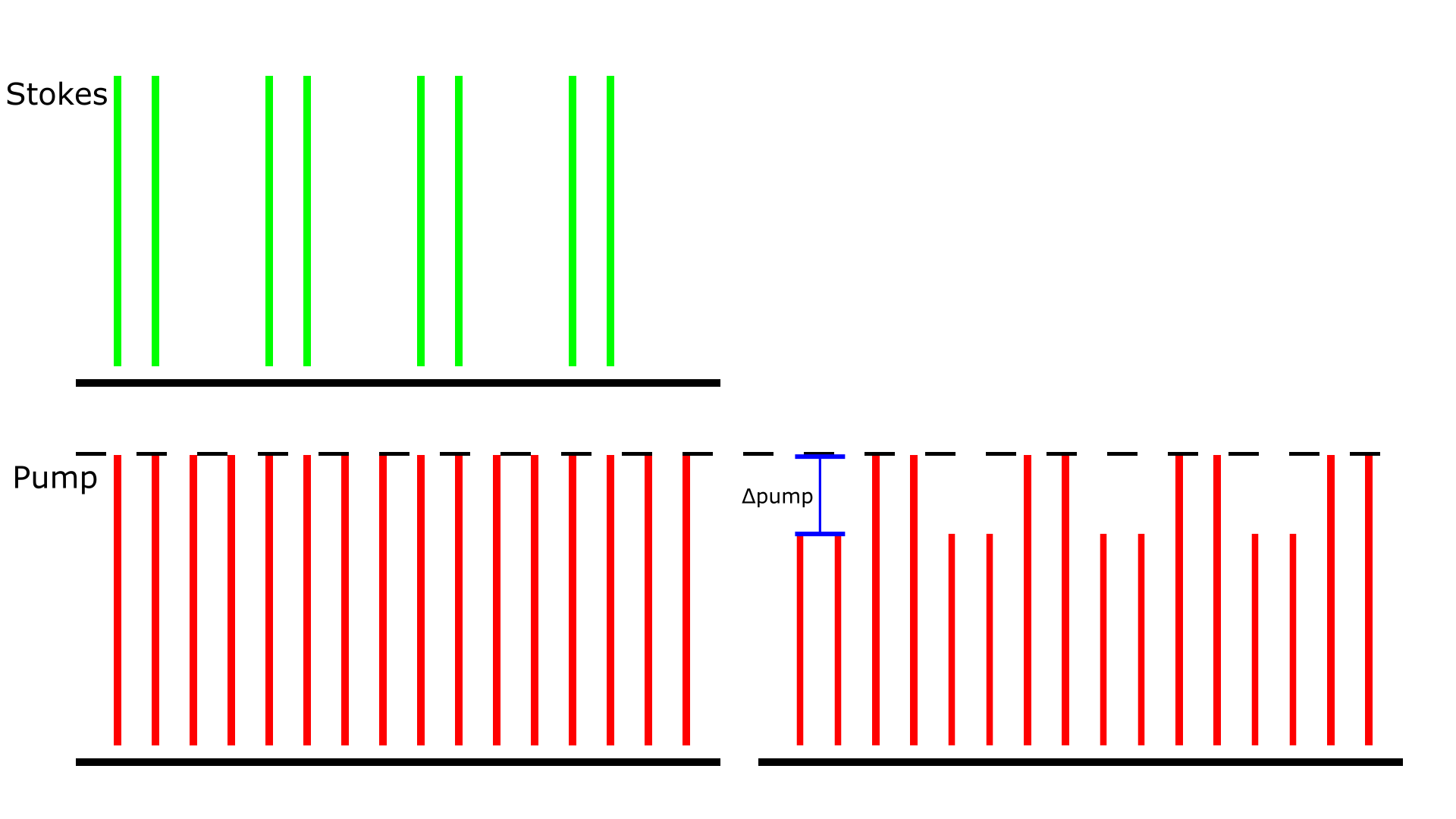 图 1:受激拉曼损耗检测方案。检测到由于受激拉曼散射 (SRS) 引起的斯托克斯光向泵浦光束的幅度调制转移。演示的泵浦光束重复率为 80 MHz,斯托克斯光束的重复率为 80 MHz,但也以 20 MHz 进行调制。在该检测方案中,激光干涉拉曼损耗 (LIA) 提取的是 Δpump 光。
图 1:受激拉曼损耗检测方案。检测到由于受激拉曼散射 (SRS) 引起的斯托克斯光向泵浦光束的幅度调制转移。演示的泵浦光束重复率为 80 MHz,斯托克斯光束的重复率为 80 MHz,但也以 20 MHz 进行调制。在该检测方案中,激光干涉拉曼损耗 (LIA) 提取的是 Δpump 光。
仪表
所用的激光系统能够输出两个 80 MHz 的激光脉冲串:斯托克斯光束的波长为 1030 nm,泵浦光束的波长为 790 nm。激光输出也用于同步调制:80 MHz 参考频率被发送到分频器以产生 20 MHz TTL 输出。这 20 MHz 输出被利用两次:一次作为电光调制器的驱动频率以调制斯托克斯光束,一次作为外部锁相环路的 LIA 输入通道 2(In B)的参考频率。泵浦光束由硅光电二极管检测,然后发送到 LIA 的输入通道 1(In A)。来自输出通道 1(Out A)的信号被发送到数据采集卡进行图像采集。来自输出通道 2(Out B)的信号被最小化(通过调整相移)。
单通道锁相放大器配置
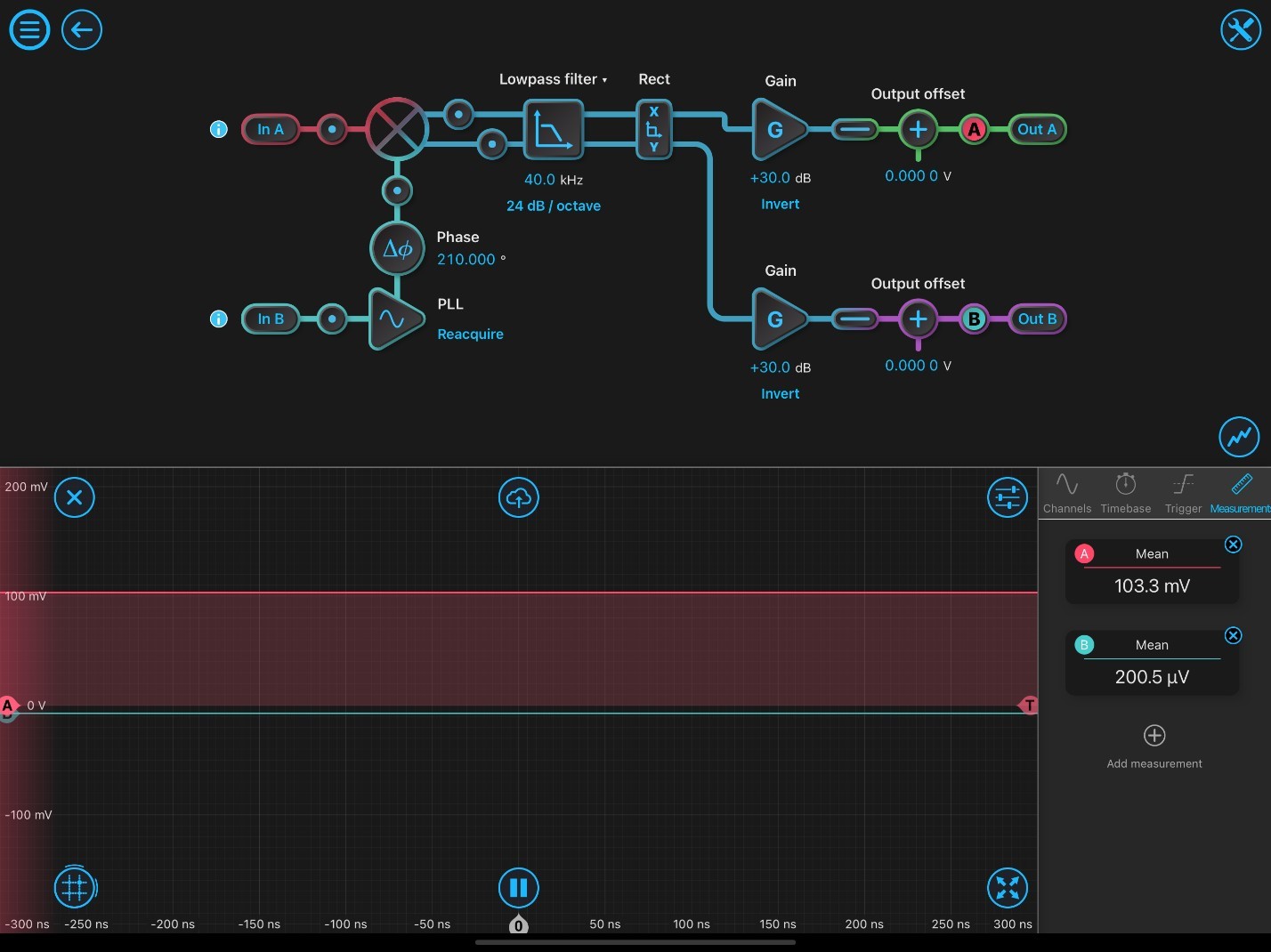 图 2:典型的锁定放大器配置设置。
图 2:典型的锁定放大器配置设置。
图 2 演示了用于 SRS 显微镜实验的 LIA 的初始设置。 在初始设置时,必须重新获取锁相环。 输入均配置为 AC:50 欧姆。 通过调整相位度数优化相移 (Df),直到 Out A 最大化(正值)并且 Out B 最小化(接近零)。 探针 A 显示对应于 DMSO 最高信号峰的 SRS 信号(2913 cm-1),并最大化输出103.3 mV,输出A。探针B指示正交输出,其最小值为零。一旦LIA针对校准溶剂进行优化,即可对样品进行成像。
 图 3:2930 cm 处的 SRS HeLa 细胞图像-1 拉曼跃迁。
图 3:2930 cm 处的 SRS HeLa 细胞图像-1 拉曼跃迁。
图 3 是使用 Moku:Pro 锁相放大器拍摄的 HeLa 细胞图像。 显示的图像是从 SRS 图像生成的,拉曼位移为 2930 cm-1,对应于蛋白质峰。 低通滤波器设置为 40 kHz,对应于 ~4 µs 的时间常数。 可以根据 SRS 信号大小增加或减少增益。
双通道成像
Moku:Pro 的 LIA 也适用于实时双色 SRS 成像。 这是通过在 SRS 成像中应用正交调制并检测 LIA 的 X 和 Y 输出来执行的。3 在这种情况下,斯托克斯调制包含两部分:一个20 MHz脉冲串,用于生成SRS信号;另一个20 MHz脉冲串,相移90°,用于生成针对不同拉曼频段的SRS信号。由于90°相移,两个通道(输出A和输出B)彼此正交,因此可以同时获取两个SRS图像而不会产生干扰。


2850厘米-1 脂质 2930 厘米-1 蛋白质
图 4:使用正交调制和输出在两个不同的拉曼跃迁下同时获得鼠脑样本的双通道 SRS 图像。
图 4 是利用双通道 X&Y 输出在 2930 cm 处生成两个 SRS 图像的代表性图像-1 和2850厘米-1 同时进行。
多仪器模式应用
在大多数 SRS 显微实验中,光谱范围限制在 300 cm 左右-1 由于激光器总带宽的限制。 绕过这一技术障碍的一种方法是使用可调谐激光器扫描波长。 然而,波长调谐速度很慢,而且对于时间敏感的实验(如活细胞成像)来说往往不够。 应对这一挑战的另一种解决方案是引入第三束激光束来扫描不同的拉曼过渡区域。 这种能力对于两个光谱区域的同时成像特别有吸引力:一个在指纹区域(例如~1600 cm-1 用于酰胺振动)和一个在 CH 区域(例如 ~2900 cm-1 蛋白质)。 在 SRL 成像方法中,实验装置由一个斯托克斯光束和两个不同波长的泵浦光束组成。 此设置的常用检测方法需要单独的检测器和单独的 LIA。 然而,Moku:Pro 的多仪器模式允许部署多个 LIA,因此可以在不需要任何额外硬件妥协的情况下实施第二个 LIA
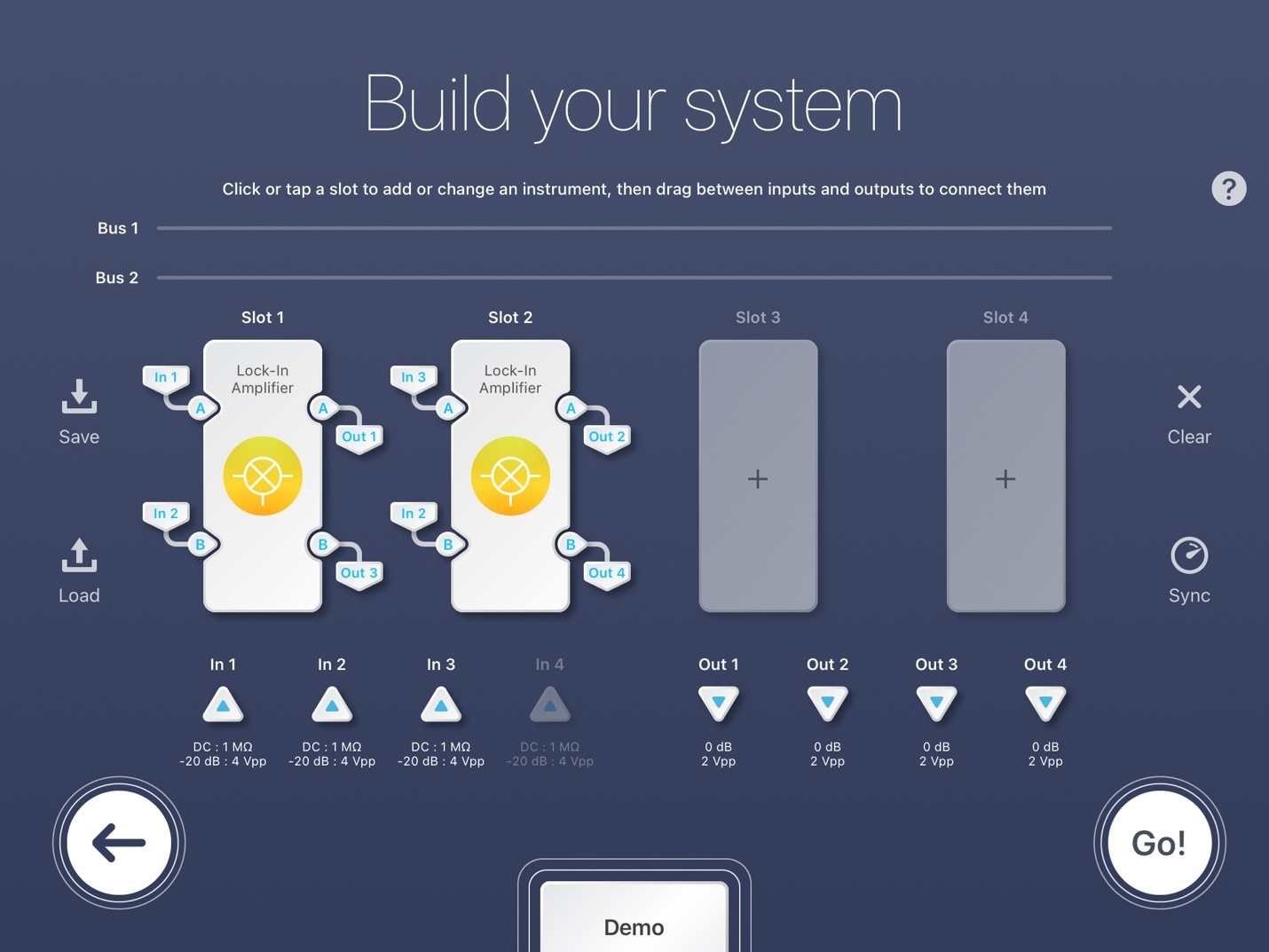 图 5:Moku:Pro 多仪器锁相放大器配置。
图 5:Moku:Pro 多仪器锁相放大器配置。
图 5 演示了 LIA 的多仪器模式设置,用于同步 SRS 显微镜实验。 对于Slot 1,In 1是第一个光电二极管的检测信号,In 2是参考信号,Out 1是发送到数据采集卡的信号,Out 3被丢弃。 对于 Slot 2,In 3 是第二个光电二极管的检测信号,In 2 再次作为参考,Out 2 是发送到数据采集卡的信号,Out 4 被丢弃。 此配置仅使用 2 个 Moku 插槽中的 4 个。 插槽 3 和 4 未分配,因此可用于进一步的 LIA 或任何其他 Moku 仪器。 输入全部配置为 AC:50 欧姆。 每个 LIA 插槽(1 和 2)都遵循与单通道 LIA 配置相同的设置。 发送到数据采集卡的每个检测到的信号(输出 1 和 2)应通过调整各自的相移来最大化。
在使用三台激光器的情况下,Moku:Pro 的多仪器模式可以配置两个锁定放大器,从而将系统简化为一台设备,且不影响性能。这使得研究人员能够同时拍摄两幅波数差异较大的 SRS 图像,并利用一台 Moku:Pro 处理两个光电二极管探测器信号。


2930厘米-1 蛋白质 2125 厘米-1 光盘
图 6:HeLa 细胞 SRS 图像使用多仪器设置在间隔较远的拉曼跃迁处拍摄。
图 6 是利用一个 Moku:Pro 处理两个光电二极管检测器信号同时拍摄两个大波数差的 SRS 图像的代表性图像。
结语
Moku:Pro 的 LIA 为大量 SRS 显微镜实验提供了出色的解决方案。 在本文档中,讨论了典型的单通道 SRS 成像、双通道成像和多仪器成像。 用户界面允许对提取低强度 SRS 信号进行直观和强大的控制。 重要的是,Moku:Pro 的多仪器工具功能允许在不妥协的紧凑型系统上进行复杂的成像实验。
 图 7:Moku:Pro 在多仪器模式下使用的图像。In 1 和 In 3 分别是插槽 1 和插槽 2 中 LIA 的信号输入。In 2 是两个 LIA 插槽的参考信号。在所示配置中,Out 1 和 Out 3 是记录信号,Out 2 和 Out 4 是插槽 1 和 2 的转储信号。
图 7:Moku:Pro 在多仪器模式下使用的图像。In 1 和 In 3 分别是插槽 1 和插槽 2 中 LIA 的信号输入。In 2 是两个 LIA 插槽的参考信号。在所示配置中,Out 1 和 Out 3 是记录信号,Out 2 和 Out 4 是插槽 1 和 2 的转储信号。
参考文献:
- 弗洛伊迪格,W。 敏,W。 萨尔,BG; 卢,S。 霍尔托姆,GR; 他,C.; 蔡,JC; 康,JX; Xie, XS,通过受激拉曼散射显微镜进行高灵敏度的无标记生物医学成像。 科学 322 (5909),1857 1861。
- 希尔,H。 Fu, D.,使用受激拉曼散射显微镜进行细胞成像。 肛门。 化学。 91 (15),9333 9342。
- 菲格罗亚, ; 胡,R。 雷纳,SG; 郑,Y。 Fu, D.,通过受激拉曼散射进行实时微尺度温度成像。 物理化学快报 11 (17),7083 7089。